
Sadržaj:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Zadnja izmjena 2025-01-22 16:56.
An jonsko jedinjenje je div struktura of joni . The joni imaju redovni, ponavljajući aranžman koji se zove an jonska rešetka . Ovo je zašto solidan jonski spojevi formiraju kristale pravilnog oblika.
Osim toga, zašto jonska jedinjenja postoje u kristalnoj rešetki?
Svojstva jonska jedinjenja sledi iz teorijskog kristalna rešetka raspored čvrsto povezanih naelektrisanih čestica koje ih čine. Jonska jedinjenja imaju tendenciju da imaju visoke tačke topljenja i ključanja, jer je privlačnost između joni u rešetka je veoma jak.
Isto tako, šta je jonska rešetka? An jonski jedinjenje se sastoji od kationa i anjona u a rešetka struktura. The jonska rešetka strukture drže zajedno elektrostatičke sile privlačenja između suprotno naelektrisanih joni . Metal ili legura metala sastoji se od metalnih kationa i mora delokalizovanih elektrona.
Ovdje su sva jonska jedinjenja kristalna?
Pojedinac joni unutar an jonsko jedinjenje obično imaju više najbližih susjeda, pa se ne smatraju dijelom molekula, već umjesto toga dijelom kontinuirane trodimenzionalne mreže, obično u kristalno struktura. Jonska jedinjenja obično imaju visoke tačke topljenja i ključanja, te su tvrdi i krti.
Koje su 4 karakteristike jonskih jedinjenja?
Evo kratke liste glavnih svojstava:
- Oni formiraju kristale.
- Imaju veće entalpije fuzije i isparavanja od molekularnih spojeva.
- Teske su.
- Oni su krhki.
- Imaju visoke tačke topljenja i visoke tačke ključanja.
- Oni provode struju, ali samo kada su otopljeni u vodi.
Preporučuje se:
Kako nacrtati Lewisovu strukturu kovalentnog jedinjenja?

Nacrtajte Lewisove simbole pojedinačnih atoma u molekulu. Povežite atome na način da oko svakog atoma smjesti osam elektrona (ili dva elektrona za H, vodonik) gdje god je to moguće. Svaki par zajedničkih elektrona je kovalentna veza koja se može predstaviti crticom
Koje su strukturne jedinice koje čine jonska jedinjenja i kako se nazivaju?

Za binarna jonska jedinjenja (jonska jedinjenja koja sadrže samo dve vrste elemenata), jedinjenja se imenuju tako što se prvo napiše ime kationa, a zatim ime anjona. Na primjer, KCl, jonsko jedinjenje koje sadrži K+ i Cl- ione, naziva se kalijum hlorid
Zašto se jonska jedinjenja lako otapaju u vodi?

Da bi rastvorili jonsko jedinjenje, molekuli vode moraju biti u stanju da stabilizuju ione koji su rezultat prekida jonske veze. Oni to rade hidratacijom jona. Voda je polarni molekul. Kada stavite jonsku tvar u vodu, molekuli vode privlače pozitivne i negativne ione iz kristala
Po čemu su sva jedinjenja slična?

Objašnjenje: Jedinjenja kao što je CO2 sastoje se od atoma spojenih da naprave stabilne molekule. Svi spojevi su uvijek napravljeni od atoma različitih tipova da bi napravili molekule. Elementi kada su molekuli uvijek su napravljeni od atoma istog tipa
Kako pišete formule za binarna jonska jedinjenja?
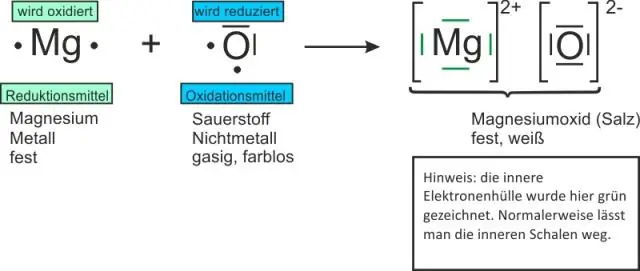
Formule za binarna jedinjenja počinju s metalom nakon čega slijedi nemetal. Pozitivni i negativni naboji moraju se međusobno poništiti. Formule jonskih spojeva su napisane korištenjem najnižeg omjera jona
