
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Zadnja izmjena 2025-01-22 16:56.
To rastvoriti an jonsko jedinjenje , the vode molekuli moraju biti u stanju stabilizirati joni koji su rezultat razbijanja jonski obveznica. Oni uradi ovo hidratacijom joni . Voda je polarni molekul. Kada postavite an jonski supstanca u vode , the vode molekule privlače pozitivne i negativne joni od kristala.
Na ovaj način, zašto je jonsko jedinjenje rastvorljivo u vodi?
Jonska jedinjenja se rastvaraju u vodi ako se energija odaje kada se joni komunicirati sa vode molekula kompenzira energiju potrebnu za razbijanje jonski veze u čvrstom stanju i energija potrebna za razdvajanje vode molekule tako da joni može se ubaciti u rastvor.
Nakon toga, postavlja se pitanje zašto su jonske veze toliko slabije kada su u vodi? Jonske veze obično su jači od kovalentnih obveznice jer tu je privlačnost između suprotno naelektrisanih joni . Ali, kada molekuli sa jonske veze rastvoreni su u vode the jonske veze postati mnogo slabiji u poređenju sa kovalentnim obveznice nakon molekula sa kovalentnim obveznice su rastvoreni u vode.
Da li se jonska jedinjenja lako rastvaraju u vodi?
Voda molekuli mogu imati snažnu interakciju sa joni , formirajući oko njih ljusku koja također zaklanja joni jedno od drugog. An jonsko jedinjenje će rastvoriti lako ako interakcija energija između joni i vode je energetski (što fizičari nazivaju slobodnom energijom) povoljnija u odnosu na čvrstu so.
Zašto su jonska jedinjenja rastvorljiva u vodi GCSE?
Jonski vezivanje Zbog jakih elektrostatičkih sila između njih, potrebna je velika energija da se odvoje pozitivni i negativni joni u kristalnoj rešetki. Ovo znači to jonska jedinjenja imaju visoke tačke topljenja i ključanja. Kada kristal od an jonsko jedinjenje se rastvara u vodi , the joni odvojeno.
Preporučuje se:
Koje su neke stvari koje se ne otapaju u vodi?

Šećer i sol su primjeri rastvorljivih supstanci. Tvari koje se ne otapaju u vodi nazivaju se nerastvorljivim. Pijesak i brašno su primjeri nerastvorljivih supstanci
Koje su strukturne jedinice koje čine jonska jedinjenja i kako se nazivaju?

Za binarna jonska jedinjenja (jonska jedinjenja koja sadrže samo dve vrste elemenata), jedinjenja se imenuju tako što se prvo napiše ime kationa, a zatim ime anjona. Na primjer, KCl, jonsko jedinjenje koje sadrži K+ i Cl- ione, naziva se kalijum hlorid
Zašto se kuhinjska so lako rastvara u vodi?

Kuhinjska sol se otapa u vodi jer vrlo polarne molekule vode privlače i pozitivno nabijene natrijeve ione i negativno nabijene kloridne ione. I druge soli se otapaju u vodi, ali neke od njih se otapaju lakše od drugih
Da li sva jonska jedinjenja imaju rešetkastu strukturu?

Jonsko jedinjenje je džinovska struktura jona. Joni imaju pravilan, ponavljajući raspored koji se naziva jonska rešetka. Zbog toga čvrsti jonski spojevi formiraju kristale pravilnog oblika
Kako pišete formule za binarna jonska jedinjenja?
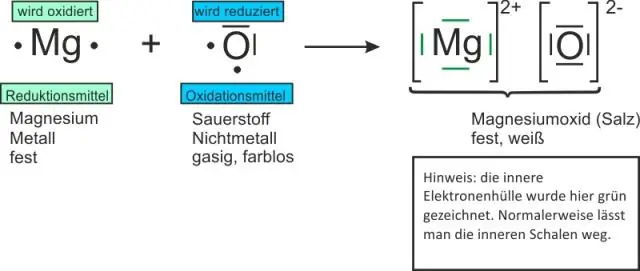
Formule za binarna jedinjenja počinju s metalom nakon čega slijedi nemetal. Pozitivni i negativni naboji moraju se međusobno poništiti. Formule jonskih spojeva su napisane korištenjem najnižeg omjera jona
