
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Zadnja izmjena 2025-01-22 16:56.
Odgovor i objašnjenje: Nitrogen je primjer a dijatomski molekula. Hemikalija formula za nitrogen gas je N2. Drugi dijatomski molekule su vodonik, kiseonik, Prema tome, koja je formula za dušik?
Hemikalija formula za azot gas je N2. Nitrogen plin je jedan od dvoatomskih elemenata, u kojem se jedan molekul sastoji od dva atoma istog elementa vezanih jednom ili više kovalentnih veza.
Osim toga, da li je dušik dvoatomski molekul? A dijatomski molekul ima dva atoma. The dijatomski elementi su vodonik, nitrogen , kiseonik, fluor, hlor, brom i jod.
Osim ovoga, šta je dvoatomski azot?
Elemental nitrogen je bezbojan, bez mirisa, bez ukusa i uglavnom inertan dijatomski gas u standardnim uslovima, koji čini 78% zapremine Zemljine atmosfere. Nitrogen javlja se u svim živim organizmima. Sastavni je element aminokiselina, a time i proteina i nukleinskih kiselina (DNK i RNK).
Zašto se azot piše kao n2?
Simbol za nitrogen je N , međutim kada nitrogen samo po sebi se upućuje u reakciji ( Nitrogen reaguje sa xxx ili xxx reaguje sa nitrogen ), mi pišemo N2 . Ovo je zbog nitrogen poznat kao dvoatomski molekul. Ovo je zbog nitrogen poznat kao dvoatomski molekul.
Preporučuje se:
Koja je konfiguracija valentnog elektrona jezgra za dušik?
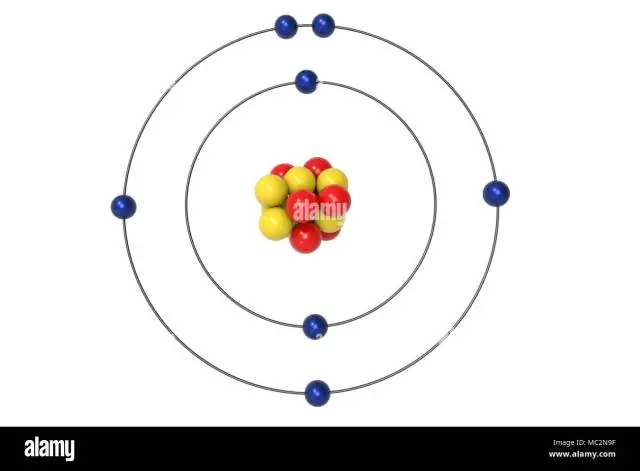
Preostala tri elektrona ići će u 2p orbitalu. Stoga će konfiguracija N elektrona biti 1s22s22p3. Konfiguracijska notacija za dušik (N) omogućava naučnicima jednostavan način da napišu i komuniciraju kako su elektroni raspoređeni oko jezgra atoma dušika
Koja je formula nepolarne molekule koja sadrži nepolarne veze?

(1), (3) H2O i NH3 su molekuli koji sadrže polarne kovalentne veze, ali njihove elektronske distribucije nisu simetrične. (4) H2 je nepolarna molekula koja ima simetričnu distribuciju elektrona, ali veza između atoma vodika je nepolarna kovalentna
Kojih je 8 dvoatomskih elemenata Šta znači biti dvoatomski?
Dvoatomski elementi su svi gasovi i formiraju molekule jer sami nemaju punu valentnu ljusku. Dvoatomski elementi su: brom, jod, azot, hlor, vodonik, kiseonik i fluor. Načini da ih zapamtite su: BrINClHOF i Have No Fear of Ice ColdBeer
Zašto se neki elementi nalaze kao dvoatomski molekuli u prirodi?

Svi dijatomski elementi su plinovi i formiraju molekule jer sami nemaju punu valentnu ljusku. Dvoatomski elementi su: brom, jod, azot, hlor, vodonik, kiseonik i fluor. Načini da ih zapamtite su: BriNClHOF i Have No Fear Of Ice ColdBeer
Zašto su važni dvoatomski molekuli?

Dijatomski elementi su igrali važnu ulogu u razjašnjavanju pojmova elementa, atoma i molekula u 19. stoljeću, jer se neki od najčešćih elemenata, kao što su vodonik, kisik i dušik, javljaju kao dvoatomski molekuli
