
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Zadnja izmjena 2025-01-22 16:56.
Kako se voda razlikuje ispod i iznad tačke topljenja to? Ispod ostaje blizu jedno od drugog i odbijaju se jedno od drugog. Iznad molekuli se još više približavaju ispod . The ključanje /kondenzacija tačka of vode je 373K.
Zbog toga, zašto su tačke topljenja i smrzavanja iste?
Zamrzavanje i topljenje su samo različiti termini koji se koriste za opisivanje prijelaza između čvrstog i tekućeg stanja materijala. Zamrzavanje obično znači da se energija uklanja iz materijala (tečnost prelazi u čvrstu) i topljenje obično znači da se energija dodaje materijalu (čvrsto tijelo prelazi u tekućinu).
Neko se takođe može zapitati da li voda ima nižu tačku topljenja? Topljenje upija toplotu ("latentna toplota") jer tečnost ima više energije od čvrste. To hladi led i slano vode na manje od 0°C. Dakle, da, to je niže stvarnu temperaturu.
Slično, možete pitati, kako ćete znati da li je tačka topljenja jedinjenja iznad ili ispod sobne temperature?
Ako the normalna tačka topljenja neke supstance je ispod sobne temperature , the supstance je tečnost na sobnoj temperaturi . Benzen topi se na 6°C i ključa na 80°C; to je tečnost na sobnoj temperaturi . Ako oba normalna tačka topljenja i normalna tačka ključanja su iznad sobne temperature , the supstance je solidan.
Koja supstanca ima višu tačku topljenja od vode?
Natrijum hlorid se topi na 801°C. Led (čvrsti H 2 O) je molekularni spoj čiji se molekuli drže zajedno vodonik obveznice. Mada vodonik veze su najjača međumolekularna sila, snaga vodonik veza je mnogo manja nego kod jonskih veza.
Tačka topljenja.
| Materijal | Tačka topljenja (°C) |
|---|---|
| gvožđe | 1538 |
Preporučuje se:
Da li nanocijevi imaju visoke tačke topljenja?

Postavka je omogućila manipulaciju pojedinačnim nanočesticama i zagrijavanje pojedinačnih CNT-a primjenom struje na njih. Utvrđeno je da CNT podnose visoke temperature, do tačke topljenja W čestica prečnika 60 nm (~3400 K)
Koje veze imaju visoke tačke topljenja?

Visoke tačke topljenja i ključanja - jonske veze su veoma jake - potrebno je mnogo energije da se one razbiju. Dakle, jonska jedinjenja imaju visoke tačke topljenja i ključanja. Provodljivi kada su tečni - joni su nabijene čestice, ali jonska jedinjenja mogu provoditi električnu energiju samo ako se njihovi ioni slobodno kreću
Da li prelazni metali imaju niske tačke topljenja?

Tačke topljenja prelaznih metala su visoke zbog 3d elektrona koji su dostupni za metalno povezivanje. Gustine prelaznih metala su visoke iz istog razloga kao i visoke tačke ključanja. Prijelazni metali su svi gusti metali sa visokim tačkama topljenja i ključanja
Da li voda ima nisku tačku topljenja?

Voda zapravo nema nisku tačku topljenja u poređenju sa drugim kovalentnim jedinjenjima. Većina kovalentnih jedinjenja male molarne mase je gasovita na sobnoj temperaturi dok je voda tečna. Kovalentne veze su dovoljno jake, ali su ograničene na pojedinačne molekule, a ne na cijeli komad spoja
Zašto voda ima visoku tačku topljenja?
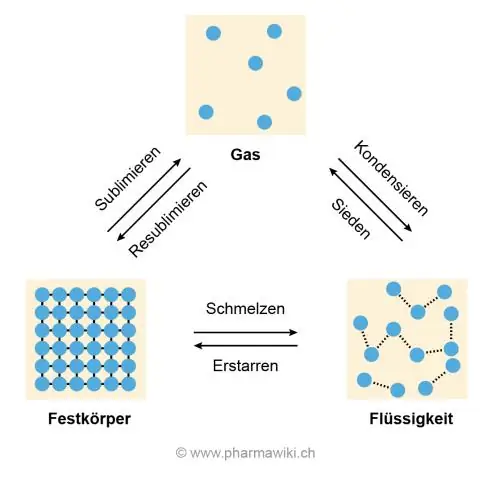
Razlog za visoke temperature topljenja i ključanja je vodonikova veza između molekula vode koja ih uzrokuje da se drže zajedno i da se odupiru razvlačenju, što se događa kada se led otopi i voda proključa i postane plin
